Gli antiossidanti sono molecole che possono neutralizzare i radicali liberi o altre specie chimiche reattive che causano lo stress ossidativo.
Gli antiossidanti possono essere presenti nell’organismo o introdotti con l’alimentazione. Essi sono importanti per prevenire o limitare i danni causati dai radicali liberi alle cellule e ai tessuti.
- Antiossidanti enzimatici – esempio superossido dismutasi, catalasi e perossidasi;
- Antiossidanti sacrificali (scavenger) – in grado di interagire con i radicali liberi accettando gli elettroni reattivi e diventando a loro volta radicali, tuttavia meno reattivi perché in grado di dislocare la carica più efficacemente; reagendo in prima persona, si consumano. Alcuni esempi sono le vitamine C ed E e il β-carotene oppure i pigmenti vegetali come i fenoli; tra queste molecole troviamo anche degli enzimi, ed i micronutrienti sono spesso fondamentali perché appartengono alla struttura di tali proteine.
- Antiossidanti preventivi – proteine che legano ioni metallici catalizzatori della reazione di Fenton; esempio transferrina, ferritina, ceruloplasmina.
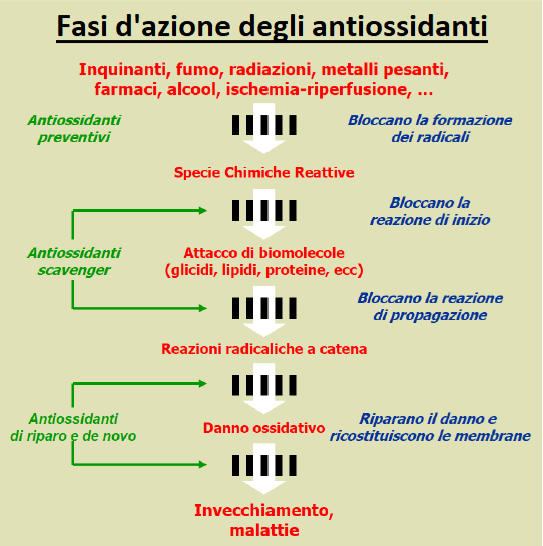
Negli organismi viventi il sistema antiossidante si suddivide prevalentemente in antiossidanti endogeni rappresentati dagli enzimi o da alcune particolari molecole come il glutatione (GSH), ed antiossidanti esogeni cui appartengono le vitamine ed i fenoli bioattivi. Possono essere sia lipofili che idrofili ed operano azione sinergica.
La superossido dismutasi trasforma lo ione superossido in acqua ossigenata, che può avere due destini: il primo è quello di essere ulteriormente dismutata da antiossidanti enzimatici a dare acqua (glutatione) o acqua e ossigeno (catalasi, ma solo in caso di quote alte poiché ha l’affinità di un enzima per il substrato (KM) molto alta); il secondo è quello di reagire con ioni metallici nella reazione di Fenton a dare ione ossidrile: gli antiossidanti cercano di evitare questa reazione chelando i metalli bivalenti, ma qualora si verifichi possono intervenire ulteriori molecole a neutralizzare tale prodotto prima che danneggi la cellula.
Gli antiossidanti si distribuiscono in diversi compartimenti cellulari: sulla membrana si trovano la vitamina E, gli acidi grassi polinsaturi (PUFA) ed il β-carotene, mentre con localizzazione citoplasmatica si ha il glutatione, il glutatione perossidasi (GPx), la Superossido dismutasi (SOD), il selenio e l’ascorbato. All’interno dei mitocondri troviamo urbichinolo, SOD, GPx, selenio e vitamina E, ed infine nei perossisomi è tipica la catalasi.
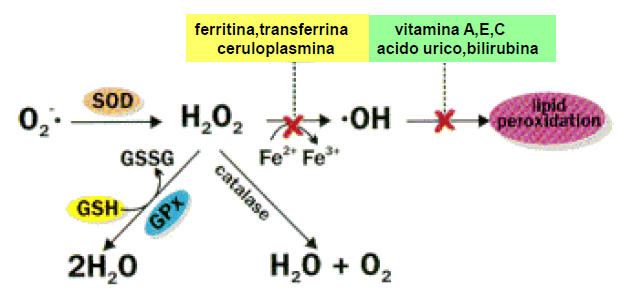
Esempi di antiossidanti
Antiossidanti scavenger
Alcuni sono endogeni, ma sono solitamente anche presenti in diversi alimenti.
- La vitamina A solitamente si trova in frutti dal colore giallo/arancio.
- La vitamina C in frutta acidula ed ortaggi.
- La vitamina E ed il licopene si trovano nel pomodoro.
- I flavonoidi si trovano in vari alimenti con abbondanza diversa, soprattutto nel tè verde e nell’olio evo.
- La vitamina C o acido ascorbico è una sostanza a basso peso molecolare, idrofila e di origine esogena; agisce da scavenger nei confronti di vari radicali tra cui perossidi, ione superossido e ione perossido. È particolarmente importante anche perché lavora in sinergia con la vitamina E, che viene da essa rigenerata.
- La vitamina E è una sostanza liposolubile che rappresenta il principale radical-scavenger delle membrane e delle lipoproteine. Essa agisce bloccando i radicali perossidici che si formano durante la perossidazione lipidica. Può essere rigenerata dall’acido ascorbico e dal GSH.
- L’acido urico è una sostanza a basso peso molecolare ed idrofila; è un potente scavenger nei confronti di vari ossidanti ed è in grado di chelare metalli di transizione (ferro e rame) pertanto previene l’ossidazione ferro-dipendente dell’ascorbato.
- L’acido lipoico è una sostanza a basso peso molecolare relativamente idrofila; si comporta da scavenger nei confronti di vari ossidanti ed è anch’esso in grado di chelare i metalli di transizione. Consente la rigenerazione delle vitamine C ed E.
- Il coenzima Q10 è una sostanza lipofila a basso peso molecolare che si comporta da scavenger nei confronti dei radicali perossilici; consente la rigenerazione dei tocoferoli.
- I polifenoli e flavonoidi sono un’ampia classe di sostanze presenti in natura che comprendono antociani ed antoxantine, e si trovano in frutta e verdura. Anno azione di scavenger nei confronti dei radicali perossido e superossido, con possibile azione anti-aterogena.
- I carotenoidi sono un gruppo di pigmenti liposolubili rossi, arancio e giallo presenti soprattutto nella frutta e vegetali; alcuni hanno attività vitaminica come il β-carotene. In virtù delle loro caratteristiche lipofile sono presenti nelle membrane cellulari e vengono veicolati dalle lipoproteine.
Essi interrompono le reazioni a catena dei radicali perossidici–azione anche sull’ossigeno singoletto – bloccandone la reattività tramite due meccanismi: trasferimento dell’elettrone e addizione del radicale alla molecola. - Lo zinco è una componente essenziale di numerosi enzimi – nei quali svolge un ruolo strutturale, di regolazione e catalitico: alcuni esempi sono l’amminoacil-RNA-sintetasi, la DNA e la RNA polimerasi, la fosfatasi alcalina, la lattico deidrogenasi, la superossido dismutasi e le carbossipeptidasi A e B. Svolge anche un’attività antiossidante, prevenendo la perossidazione lipidica e riducendo la formazione dei radicali liberi.
Sei alla ricerca di un biologo nutrizionista nelle province di Padova o Venezia per consigli sugli antiossidanti?
CONTATTAMI!


